Od idei do terapii

Technik laboratoryjny przygotowuje preparat mikroskopowy, ustawiając szkiełko na stoliku mikroskopu. Fot. Shixart1985 / Wikimedia Commons, CC BY 2.0.
Badania kliniczne to kluczowy etap przekładania osiągnięć naukowych na innowacyjne terapie. Tu odpowiedzialność za ludzkie zdrowie i życie jest na każdym kroku.
Bez badań klinicznych nie mielibyśmy aptek na każdym rogu z regałami wypełnionymi sprawdzonymi lekami. Nie mielibyśmy rozbudowanych ulotek wyjaśniających nam dawkowanie i ostrzegających przed ewentualnymi skutkami ubocznymi, a lekarze musieliby jak przed stuleciami leczyć „na oko”. Badania kliniczne to fundament medycyny, bo pozwalają na zweryfikowanie skuteczności nowych leków, terapii i procedur medycznych.
To procesy złożone, długotrwałe i obostrzone licznymi procedurami nie ze względu na upodobanie do biurokracji, ale dla maksymalizacji bezpieczeństwa pacjentów, etyki i właściwej oceny tego, czy nowa terapia naprawdę działa.
Dlaczego badania kliniczne trwają tak długo?
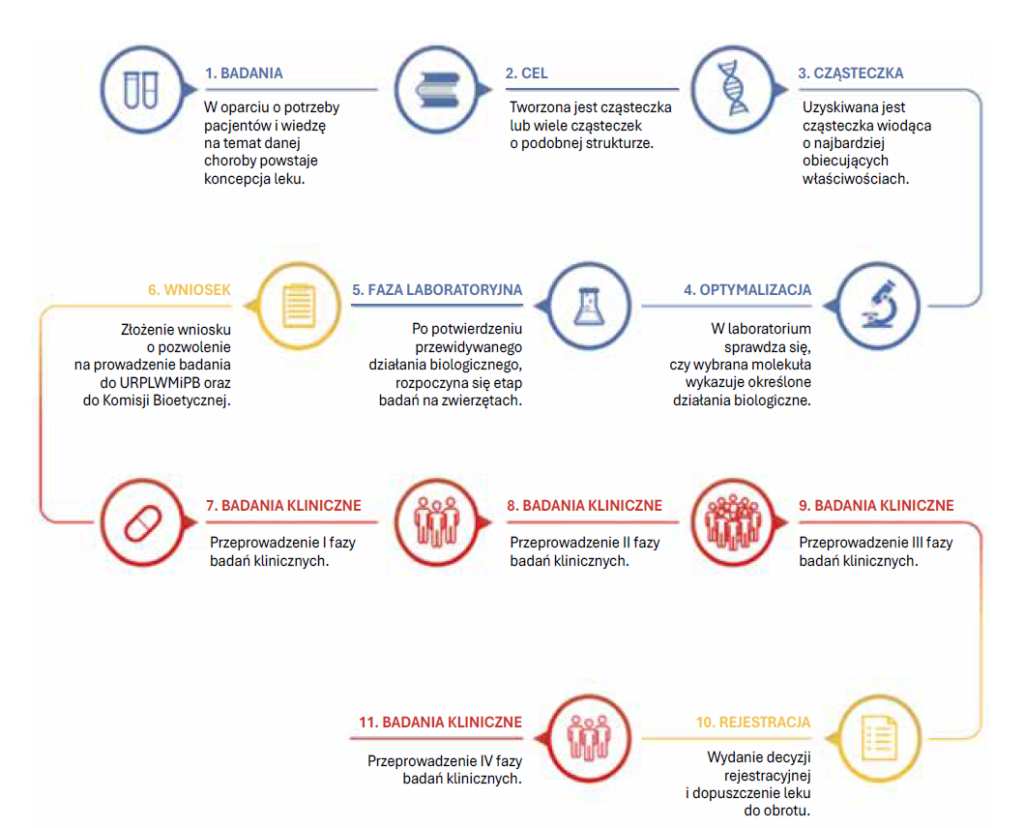
Badania kliniczne od pomysłu do rejestracji leku trwają zwykle 10–15 lat (ryc. 1). Każde badanie kliniczne jest precyzyjnie planowane przez interdyscyplinarne zespoły specjalistów (m.in. lekarzy, farmaceutów, statystyków i ekspertów od etyki). Zanim pacjent otrzyma badany produkt, substancja przechodzi przez fazy badań przedklinicznych – w laboratoriach i na modelach zwierzęcych – a dopiero po uzyskaniu pozytywnych wyników może zostać poddana badaniom z udziałem ludzi. Badanie nowych leków obejmuje ocenę bezpieczeństwa i dawkowania, weryfikację skuteczności, a na koniec wnikliwą obserwację w populacji docelowej. Każde badanie kliniczne musi uzyskać m.in. zgodę niezależnej komisji bioetycznej, czyli zespołu ekspertów, którzy oceniają, czy badanie jest bezpieczne, potrzebne i prowadzone z poszanowaniem praw pacjentów.
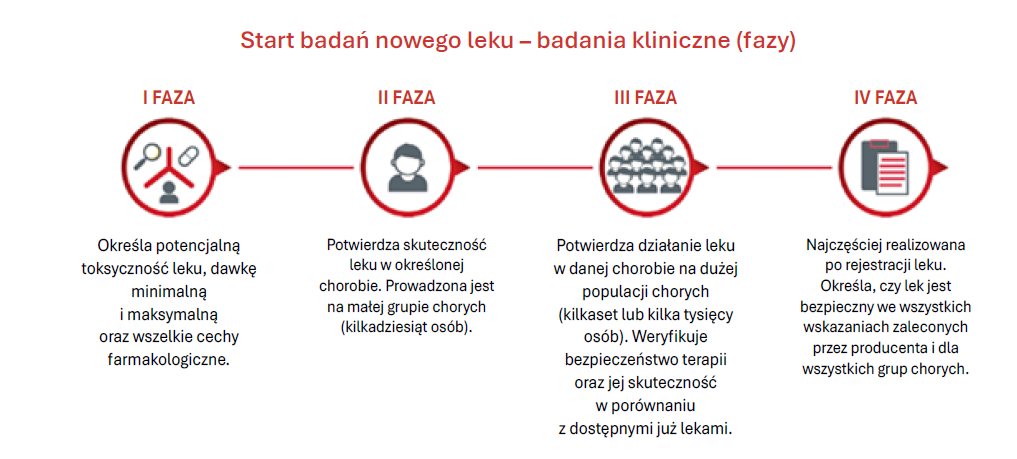
Badania z udziałem pacjentów obejmują rekrutację uczestników, realizację procedur medycznych zgodnie z protokołem, systematyczne monitorowanie bezpieczeństwa i postępów oraz analizę wyników (ryc. 2). Proces ten może w niektórych przypadkach rozpoczynać się od tzw. fazy 0 – wstępnych, pilotażowych badań na bardzo małych grupach zdrowych ochotników, pozwalających wcześnie ocenić zachowanie leku w organizmie człowieka i porównać je z wynikami badań przedklinicznych. Choć faza 0 nie ma celu terapeutycznego i nie jest obowiązkowa, dostarcza wstępnych danych farmakokinetycznych i farmakodynamicznych (czyli dotyczących losów leku w organizmie oraz jego działania na organizm), co może pomóc w szybszym podejmowaniu decyzji o dalszym rozwoju projektu. Wszystkie etapy są skrupulatnie dokumentowane i poddawane audytom oraz kontroli jakości (zarówno wewnętrznej – w ramach sponsora czy ośrodka badawczego – jak i zewnętrznej, np. przez Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych (URPL), komisje bioetyczne czy międzynarodowe instytucje regulacyjne). Dopiero pozytywny wynik określonej fazy umożliwia przejście do następnej, co istotnie wydłuża cały proces, ale jest niezbędne, by zapewnić bezpieczeństwo pacjentom oraz rzetelność uzyskanych wyników.
Jak wygląda system bezpieczeństwa i kontroli?
Współczesne badania kliniczne opierają się na pełnym poszanowaniu godności i praw uczestników, którzy są partnerami procesu badawczego. W praktyce oznacza to, że każdy pacjent otrzymuje rzetelną informację, wyraża świadomą zgodę i może w każdej chwili zrezygnować z udziału bez konsekwencji dla dalszego leczenia. Jeszcze kilkadziesiąt lat temu takie standardy nie były oczywiste – brak jasnych regulacji prowadził do nadużyć i utraty zaufania. Dlatego dziś obowiązują międzynarodowe zasady (np. Deklaracja helsińska, GCP), które gwarantują bezpieczeństwo pacjentów i przejrzystość całego procesu. Co ważne, udział w badaniu klinicznym nie jest eksperymentem, lecz jedną z najbardziej kontrolowanych i ustandaryzowanych form poszukiwania nowych rozwiązań medycznych. Każdy projekt badawczy przechodzi wieloetapową ocenę, otrzymuje pozytywną opinię komisji bioetycznej oraz zgodę URPL, a uczestnicy są szczegółowo informowani o celu, ryzyku i przebiegu badania.
Ważnym elementem transparentności jest zgłaszanie badań klinicznych w międzynarodowych rejestrach, takich jak europejski centralny system elektroniczny (Clinical Trials Information System – CTIS) czy uznawany na całym świecie ClinicalTrials.gov. Rejestracja umożliwia dostęp do kluczowych informacji o prowadzonych projektach, ich celach, metodach i wynikach. Dzięki temu każdy – od lekarza, przez badacza, po pacjenta i jego rodzinę – może sprawdzić, jakie badania się toczą, jaki mają cel i na jakim są etapie. Co więcej, każda zmiana mogąca mieć wpływ na bezpieczeństwo uczestników musi być natychmiast raportowana do instytucji nadzorczych, a w razie potrzeby prowadzi do modyfikacji lub nawet przerwania badania. O tym ostatnim mogą decydować sami badacze lub sponsor, a w przypadku większych projektów – także niezależny komitet monitorujący. Badania mogą być też wstrzymane przez instytucje regulacyjne, jeśli uznają, że uczestnicy są narażeni na zbyt duże ryzyko. Wpis do międzynarodowych rejestrów ma znaczenie nie tylko informacyjne dla pacjentów i lekarzy, lecz także ostrzega inne zespoły badawcze przed potencjalnymi zagrożeniami. Tak wielopoziomowy system kontroli sprawia, że innowacyjne terapie wprowadzane w ramach badań klinicznych cechują się wysokim poziomem bezpieczeństwa.
Rozwój niekomercyjnych badań klinicznych w Polsce
Badania kliniczne mogą być finansowane zarówno przez przemysł farmaceutyczny, jak i przez instytucje publiczne. Rola państwa w tym procesie nie jest dodatkiem – jest warunkiem niezbędnym do zapewnienia równości w dostępie do terapii i rozwoju nauki. Dlatego w 2019 roku powołano Agencję Badań Medycznych (ABM) – instytucję publiczną, która uzupełniła istniejącą lukę w systemie ochrony zdrowia: niekomercyjnych badań klinicznych.
Rolą agencji jest finansowanie i wspieranie takich projektów, które nie są motywowane zyskiem, lecz zidentyfikowanymi przez naukowców lukami w wiedzy, potrzebami społecznymi i zdrowotnymi obywateli. Badania te mają na celu poszerzenie wiedzy medycznej, weryfikację rozwiązań systemowych i ostatecznie mają prowadzić do zmian w refundacji, dostępności terapii i wytycznych klinicznych, nawet jeśli ich zakres obejmuje rzadkie schorzenia. Dzięki niekomercyjnym badaniom klinicznym możliwe jest podejmowanie decyzji na szczeblu rządowym opartych na rzetelnych dowodach, często o mniejszym znaczeniu biznesowym.
Co ważne, badania niekomercyjne w naszym kraju dynamicznie zyskują na znaczeniu. W latach 2018– 2019 w Polsce zarejestrowano aż 970 badań komercyjnych i zaledwie 26 niekomercyjnych – te ostatnie stanowiły 2,6 proc. wszystkich projektów. Jednak już w latach 2020–2021 liczba zarejestrowanych niekomercyjnych badań wzrosła do 66, a ich udział w rynku sięgnął 5,6 proc., co oznacza ponaddwukrotny wzrost.
Rok 2021 był pod tym względem rekordowy – zgłoszono aż 729 badań klinicznych, z czego 41 dotyczyło projektów niekomercyjnych. Co szczególnie istotne, aż 40 zostało sfinansowanych przez ABM. Finansowane badania dotyczą przede wszystkim chorób rzadkich, psychiatrii, neurologii oraz powszechnych chorób cywilizacyjnych. Ich celem jest sprawdzenie, jak działają leki i wyroby medyczne w praktyce, a także opracowanie nowych sposobów diagnozowania i leczenia pacjentów. Na przykład sprawdza się, czy ambroksol – lek znany z syropów na kaszel – może pomóc osobom z rzadką chorobą Gauchera, a także czy lek wspierający układ odpornościowy (pembrolizumab) może pomóc chorym z rzadkim i trudnym do leczenia nowotworem nadnerczy. Projekty są obecnie w toku, a pierwszych wyników można się spodziewać najwcześniej w 2026 roku.
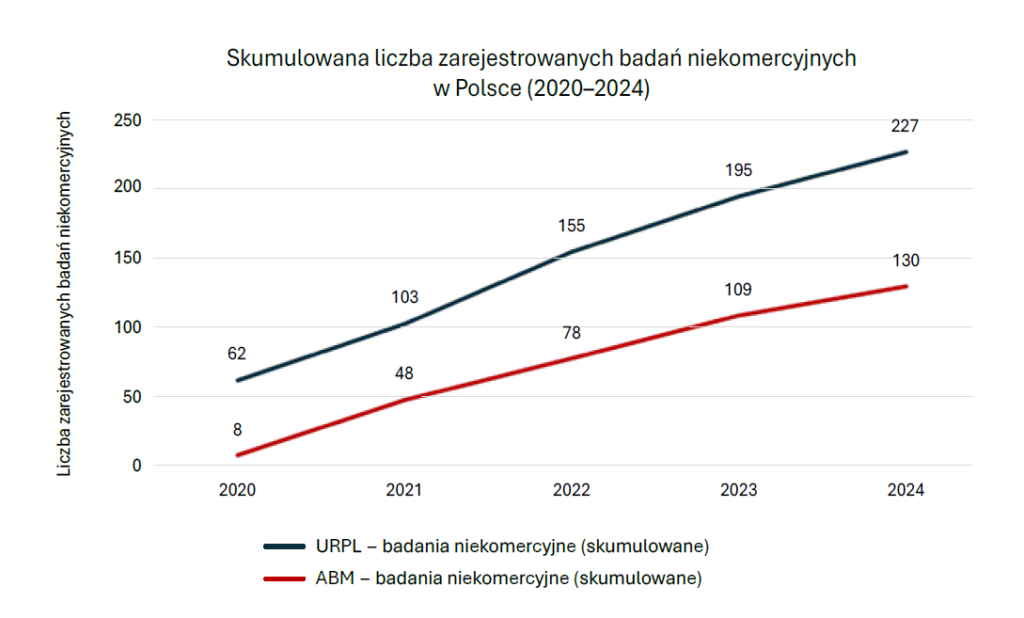
Dane za lata 2020–2024 potwierdzają tę tendencję: spośród 227 zarejestrowanych w Polsce badań niekomercyjnych 130 było realizowanych dzięki wsparciu ABM, co stanowi niemal 60 proc. To pokazuje, jak istotną rolę odgrywa Agencja Badań Medycznych w rozwoju segmentu badań prowadzonych z myślą o potrzebach pacjentów i aspektach ekonomicznych wynikających nie ze sprzedaży leków, ale z lepszego funkcjonowania społeczeństwa.
Zwrócenie uwagi na pomijanych. Rola badań niekomercyjnych
Niekomercyjne badania kliniczne to projekty prowadzone przez lekarzy i naukowców, a nie przez firmy farmaceutyczne. Ich celem nie zawsze jest opracowanie nowego leku, ale często sprawdzenie, czy znane terapie mogą być skuteczne w innych chorobach, porównanie różnych metod leczenia czy dostosowanie terapii do szczególnych potrzeb pacjentów. Na przykład po dodatkowych badaniach może się okazać, że lek stosowany dotąd w leczeniu białaczki może pomóc także w terapii rzadkiego nowotworu u dzieci albo że dwa podobne leki działają tak samo skutecznie – tylko jeden jest tańszy i łatwiej dostępny. Tak było np. z semaglutydem (Ozempic), który początkowo stosowano w cukrzycy, a dziś potwierdzono jego skuteczność w leczeniu otyłości i chorób serca. Podobnie empagliflozyna, również lek przeciwcukrzycowy, okazała się skuteczna w terapii niewydolności serca i chorób nerek. W Polsce finansowane przez ABM badania sprawdzają np. zastosowanie bortezomibu u dzieci z ostrą białaczką czy walacyklowiru u kobiet w ciąży, by chronić noworodki przed zakażeniem wirusem CMV.
Tego typu optymalizacja w skali społecznej nie leży w bezpośrednim obszarze zainteresowań firm farmaceutycznych, ale ma ogromne znaczenie dla systemu ochrony zdrowia i dla pacjentów – pozwala np. obniżyć koszty terapii, poprawić komfort leczenia czy zwiększyć dostęp do skutecznych metod. Co więcej, generuje bezcenne dane, które pomagają lepiej planować politykę zdrowotną i podnosić jakość opieki medycznej w dłuższej perspektywie.
To właśnie dzięki takim badaniom jest budowany system opieki zdrowotnej oparty na dowodach (evidence-based medicine) – niezależny, przejrzysty i ukierunkowany na realne korzyści dla społeczeństwa. Polska zajmuje piąte miejsce w Unii Europejskiej pod względem liczby prowadzonych badań klinicznych, co pokazuje rosnący potencjał krajowego środowiska badawczego. Wysoka pozycja w tym rankingu sprzyja zwiększeniu dostępu pacjentów do innowacyjnych terapii oraz wzmocnieniu roli Polski w międzynarodowej współpracy naukowej.
ABM szczególną uwagę poświęca tym grupom pacjentów, które bywają pomijane przez komercyjnych sponsorów, bo nie gwarantują szybkiego zwrotu z inwestycji. To m.in. dzieci z rzadkimi nowotworami kości, pacjenci ze stwardnieniem guzowatym, kobiety w ciąży narażone na zakażenie wirusem CMV czy osoby wymagające innowacyjnych terapii, takich jak CAR-T. To właśnie przykłady badań, które trudno byłoby zrealizować bez finansowania publicznego. Od początku działalności agencja sfinansowała ponad 150 niekomercyjnych badań klinicznych, angażując ponad 1,5 mld zł i obejmując opieką kilkadziesiąt tysięcy pacjentów w całej Polsce. Finansowane projekty to zarówno duże badania prowadzone w wielu szpitalach jednocześnie, jak i mniejsze projekty sprawdzające nowe sposoby leczenia w rzadkich chorobach.
Choroby rzadkie – społeczna odpowiedzialność w praktyce
Jednym z najlepszych przykładów społecznej odpowiedzialności nauki są badania w obszarze chorób rzadkich. Prowadzenie badań w tej grupie chorych wiąże się ze szczególnymi wyzwaniami, głównie ze względu na ograniczoną liczbę pacjentów i często niejednorodny przebieg choroby. Mimo trudności badania tego typu są kluczowe dla opracowania skutecznych terapii tam, gdzie brakuje standardowych metod leczenia. Badania te często stanowią dla pacjentów jedyną szansę na dostęp do nowoczesnych terapii, a ich realizacja ma istotne znaczenie dla poprawy jakości życia osób dotkniętych chorobami rzadkimi. Ze względu na niską liczbę pacjentów i często wysokie koszty rozwoju terapii jest to obszar często pomijany przez sektor prywatny.
Właśnie tu kluczowe jest wsparcie z budżetu państwa. W Polsce działania z obszaru badań leków na choroby rzadkie realizuje Narodowe Centrum Badań i Rozwoju (mechanizm STEP i planowany program Medistrateg) oraz ABM (program Transmed, abm.gov.pl/pl/o-nas/dzialalnosc/plan-finansowy-i-plan-d/plan-dzialalnosci/2025/2929,2025.html).
Rosnące zaangażowanie państwa oraz współpraca nauki z biznesem umożliwiają wdrażanie innowacji, które poprawiają dostęp do skutecznych terapii i podnoszą jakość leczenia. Dzięki temu pacjenci szybciej zyskują dostęp do nowoczesnych leków i technologii medycznych, szpitale mogą wdrażać bardziej zaawansowane metody diagnostyczne, a lekarze – prowadzić badania, które w warunkach czysto komercyjnych często nie miałyby szans na realizację. To partnerstwo pozwala też przenosić odkrycia z laboratoriów do praktyki klinicznej, co bezpośrednio przekłada się na lepsze rokowania chorych.
Placebo – etyka i bezpieczeństwo
Stosowanie placebo w badaniach klinicznych budzi emocje, jednak obecnie jest ono wykorzystywane tylko tam, gdzie nie istnieje skuteczna terapia. Zdecydowana większość badań porównuje nową terapię ze standardową. W takim wypadku placebo i badany lek są dodatkami do standardu leczenia – w efekcie pacjenci przydzieleni do grupy placebo uzyskują co najmniej taką samą opiekę medyczną jak pacjenci leczeni na tę samą chorobę, ale nieuczestniczący w badaniu. Zdarza się, że w trakcie badania pojawią się wyraźne dowody przewagi skuteczności produktu badanego. Wówczas możliwe jest wcześniejsze zakończenie badania lub przeniesienie uczestników z grupy placebo do grupy otrzymującej produkt badany. Dzięki temu minimalizuje się ryzyko dla pacjentów i maksymalizuje szansę na szybki dostęp do skutecznego leczenia (R. Zaręba, Stosowanie placebo w badaniach klinicznych–aspekty prawne i etyczne, 2024).
Kto może wziąć udział w badaniu i na jakich warunkach?
Uczestnictwo w badaniu klinicznym jest zawsze poprzedzone dokładną kwalifikacją. Kryteria włączenia i wyłączenia opisują, kto może być uczestnikiem badania, biorą pod uwagę m.in. wiek, stan zdrowia, przebieg choroby czy wcześniejsze leczenie. Przed przystąpieniem do badania każdy uczestnik otrzymuje szczegółowe informacje o potencjalnych korzyściach, ryzykach oraz innych możliwych alternatywach. Zgoda na udział w badaniu musi zostać wyrażona przez pacjenta w pełni świadomie i dobrowolnie, a do tego ma on prawo wycofać się na każdym etapie bez konieczności podawania przyczyny.
Pacjenci zainteresowani udziałem w badaniach klinicznych mogą uzyskać dostęp do innowacyjnych rozwiązań medycznych, a przy tym odegrać aktywną rolę w rozwoju medycyny. Jednym z kluczowych źródeł informacji jest oficjalny portal Pacjent w Badaniach Klinicznych (pacjentwbadaniach.abm.gov.pl/pwb/), prowadzony przez Agencję Badań Medycznych oraz partnerów. Strona ta stanowi kompleksowe kompendium wiedzy na temat badań klinicznych. Można tam znaleźć informacje, jak wyszukać badanie kliniczne, wskazówki dotyczące udziału, odpowiedzi na najczęstsze pytania oraz przegląd dostępnych wyszukiwarek badań klinicznych.
Żeby uzyskać dostęp do badań klinicznych, pacjent lub opiekun powinien w pierwszej kolejności skonsultować się z lekarzem prowadzącym, który jest zazwyczaj najlepszym źródłem informacji. Jeżeli w ten sposób nie zdobędzie odpowiedzi na pytania, warto samodzielnie skorzystać z dostępnych wyszukiwarek badań klinicznych, które zawierają podstawowe dane o celu badania, populacji uczestników i lokalizacji ośrodków. Może być także pomocne śledzenie informacji publikowanych przez organizacje pacjenckie, stowarzyszenia oraz instytucje zajmujące się ochroną zdrowia. Warto również zapoznać się z informacjami Krajowego Centrum Bioetyki (kcb.abm.gov.pl/), gdzie przedstawiono m.in. etyczne i prawne aspekty udziału w badaniach klinicznych.
Realna zmiana
Badania kliniczne to most między odkryciem naukowym a realną pomocą dla pacjenta. W trosce o pacjenta nauka realizuje swoją społeczną odpowiedzialność – w działaniu, nie w deklaracjach.
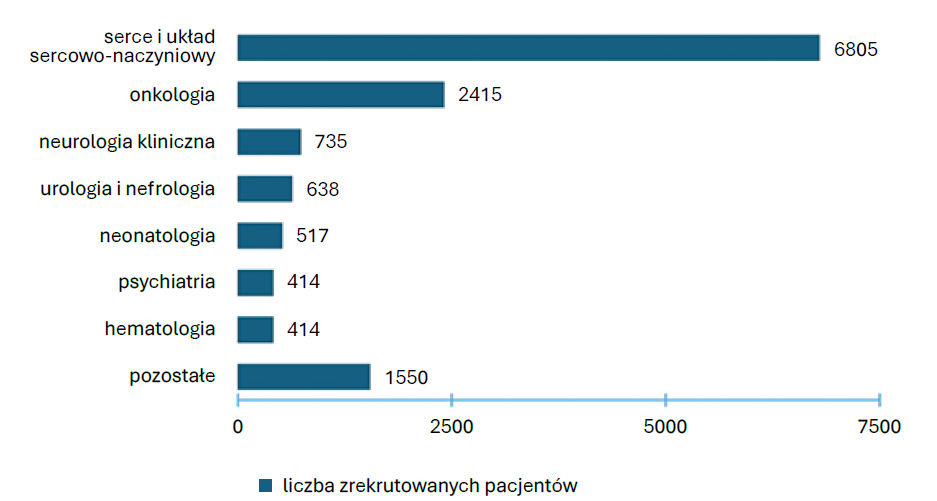
Liczba zrekrutowanych pacjentów w badaniach klinicznych w latach 2020–2025 według wskazań terapeutycznych (na podstawie raportów projektowych ABM)
Chcesz wiedzieć więcej?
- Badania kliniczne. Praktyka, prawo, etyka, T. Brodniewicz, A. Jędrzejowski (red.), Warszawa 2024.
- Czarkowski M., Czy istnieje konflikt między dobrem a prawdą w praktyce medycznej? O prawie pacjenta do wiedzy i niewiedzy, „Etyka” 2024
- Czarkowski M., Rola pacjentów w opiniowaniu badań klinicznych produktów leczniczych, „Medycyna Praktyczna” 3/2023
- Dyrektywa Komisji nr 2005/28/WE z dnia 8 kwietnia 2005 r. ustalająca zasady oraz szczegółowe wytyczne dobrej praktyki klinicznej w odniesieniu do badanych produktów leczniczych (…), Dz.Urz. UE 2005 L 91.
- Kitala D., Kaczmarska K., Kornacka J., Górski K., Bylina E., Nowak K., Staszewski R., Nowak-Życzyńska Z., Fendler W., Medical research agency: 5 years of reshaping the clinical trials ecosystem in Poland, „The Lancet Regional Health – Europe” 2024, vol. 48
- Konsultacje etyczne w praktyce klinicznej, J. Różyńska (red.), Warszawa 2023.




