Mikrobiologia
Zrozumienie jednego z mechanizmów wirulencji bakterii Porphyromonas gingivalis może pomóc w opracowaniu lepszych metod zapobiegania i leczenia paradontozy oraz związanych z nią chorób.
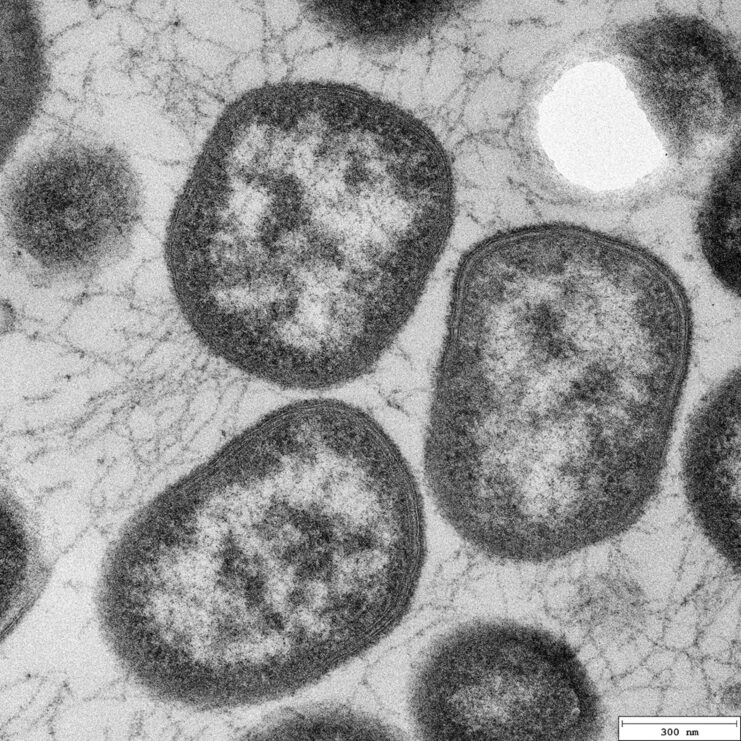
Ciało zdrowego zasiedlają liczne bakterie, które razem tworzą jego mikrobiom. Bakterie te mogą dostarczać ważne składniki odżywcze, ułatwiać trawienie pokarmu czy chronić przed infekcjami. Jednak w wyniku pojawienia się niekorzystnych warunków, takich jak pogorszenie stanu zdrowia, nieodpowiednia dieta, używki, stres, starzenie się czy czynniki genetyczne, skład mikrobiomu może się zmieniać. Wtedy to bakterie, które są naturalnym, nieszkodliwym składnikiem mikrobiomu zdrowego organizmu, mogą stać się patogenne i zastąpić częściowo bakterie korzystne, prowadząc do rozwoju chorób. Jednym z najbardziej zróżnicowanych mikrobiomów jest mikrobiom jamy ustnej. Zaburzenia w jego obrębie mogą prowadzić do chorób tkanek otaczających zęby, których przykładem jest zapalenie przyzębia, zwane potocznie paradontozą. W trakcie rozwoju paradontozy poniżej linii dziąseł tworzy się biofilm – wielowarstwowa struktura zbudowana z komórek bakterii i ich wydzielin. W jego skład wchodzi wiele gatunków bakterii. Za najważniejsze dla rozwoju paradontozy uważa się bakterie z gatunku Porphyromonas gingivalis. Jest to bakteria beztlenowa o specyficznej dla tzw. bakterii Gram-ujemnych budowie, której poznanie jest istotne, by zrozumieć kolejne części artykułu. Bakterie te zazwyczaj są pokryte otoczką zbudowaną z cukrów (choć nie wszystkie!), pod którą znajduje się błona zewnętrzna. Pod nią występuje warstwa wodna zwana peryplazmą z zanurzoną w niej ścianą komórkową, a dalej jest zlokalizowana błona wewnętrzna otaczająca pozostałą część komórki (cytoplazmę). Ściana komórkowa bakterii Gram-ujemnych jest na tyle cienka, że nie barwi się trwale fioletem krystalicznym. Dla porównania ściana komórkowa bakterii, które są zwane Gram-dodatnimi, jest gruba i barwi się fioletem krystalicznym, ale bakterie te nie posiadają błony zewnętrznej.
Bakterie P. gingivalis potrzebują do wzrostu peptydów, cząsteczek pochodzących z rozkładu białek, a także hemumolekuły zawierającej żelazo, która jest uwalniana z białek gospodarza (np. hemoglobiny). Już w stosunkowo niewielkich ilościach bakterie te mogą zaburzać funkcjonowanie układu odpornościowego człowieka, wzmagać stan zapalny oraz zakłócać równowagę w mikrobiomie jamy ustnej.

MARIUSZ MADEJ, OLGA BARCZYK-WOŹNICKA (INSTYTUT ZOOLOGII I BADAŃ BIOMEDYCZNYCH UJ)
Powodowana przez nie paradontoza prowadzi nie tylko do cofania się dziąseł, degradacji kości i w skrajnych przypadkach do utraty zębów. Stan zapalny utrzymujący się przy tej chorobie może również rozprzestrzeniać się do innych części ciała i przyczyniać się do rozwoju wielu chorób. Wyniki badań ostatnich kilkunastu lat sugerują silny związek między paradontozą a zwiększonym ryzykiem wystąpienia m.in. cukrzycy, reumatoidalnego zapalenia stawów, zachłystowego zapalenia płuc, chorób układu krążenia, niektórych nowotworów czy komplikacji w okresie ciąży. Ponadto biocząsteczki produkowane przez tę bakterię znaleziono w wielu obszarach mózgu osób cierpiących na chorobę Alzheimera. Zrozumienie, w jaki sposób bakteria powoduje tak wiele problemów w organizmie człowieka, a także poznanie narzędzi, którymi się posługuje, to ważny krok w opracowaniu skutecznej metody jej zwalczania.
Bogaty arsenał
Za patogenny potencjał P. gingivalis odpowiadają produkowane przez te bakterie różnorodne czynniki wirulencji. Tak naukowcy nazywają zestaw bakteryjnych narzędzi, który umożliwia im przeprowadzanie ataku na organizm gospodarza. W przypadku P. gingivalis chodzi o zdolność do kolonizacji jamy ustnej, niszczenie tkanek okołozębowych oraz walkę z układem odpornościowym gospodarza. Tymi czynnikami sią różne cząsteczki i struktury wykształcone przez bakterie. Wiele z nich jest związanych z powierzchnią mikroorganizmu. Pierwszym z takich narzędzi jest już najbardziej zewnętrzna warstwa bakterii, zwana otoczką. Jest to śluzowata struktura złożona głównie z cząsteczek cukrów, która pokrywa komórkę, chroniąc ją przed czynnikami środowiska. Ponadto utrudnia również rozpoznanie mikroorganizmu przez układ odpornościowy. Jej obecność nie tylko hamuje usuwanie patogenu z organizmu, lecz także wspomaga tworzenie wcześniej wspomnianych biofilmów. Innym elementem budulcowym komórki są cząsteczki lipopolisacharydu (LPS). Są one składnikami błony zewnętrznej bakterii Gram-ujemnych. W istotny sposób wpływają na stabilność tej struktury. LPS pobudza układ odpornościowy, prowadząc do rozwoju stanu zapalnego. Do innych czynników wirulencji należą enzymy tnące inne białka, czyli proteazy. Ich zadaniem jest cięcie białek gospodarza do krótszych fragmentów zwanych peptydami. Najlepiej zbadanymi proteazami, które produkuje P. gingivalis, są gingipainy. Także one są zlokalizowane na powierzchni komórki, chociaż mogą być również wydzielane do otoczenia bakterii. Gingipainy odpowiadają m.in. za niszczenie białek układu odpornościowego gospodarza. Ponadto to właśnie gingipainy odgrywają najprawdopodobniej kluczową rolę w neurotoksycznym działaniu tego patogenu. Wyniki badań prowadzonych m.in. w naszym laboratorium sugerują, że gingipainy mogą trawić obecne w komórkach nerwowych białka, co prowadzi do ich uszkodzenia. Ten neurotoksyczny efekt można obserwować w chorobie Alzheimera.

Na powierzchni bakterii znajdują się także włosowate struktury zwane fimbriami. Są to elementy budowy komórki, których zadaniem jest wiązanie (adhezja) do różnych cząsteczek w jamie ustnej (można je sobie wyobrazić jako lepkie nici). Wiążą się one do białek obecnych w kieszonkach dziąsłowych, a także występujących na powierzchni komórek tworzących tkanki otaczające zęby. Fimbrie, kontaktując się z komórkami układu odpornościowego, mogą także pobudzać je do działania. Badania na myszach wskazują, że stan zapalny, który zapoczątkowują te elementy bakterii, może prowadzić do degradacji kości wyrostka zębodołowego, czyli struktury, która utrzymuje korzenie zębów. Fimbrie aktywują również komórki wyściełające ściany naczyń krwionośnych. Może to prowadzić do tworzenia blaszki miażdżycowej i rozwoju miażdżycy naczyń. Te bakteryjne struktury pośredniczą także w agregacji komórek P. gingivalis z komórkami innych bakterii, w wyniku czego może dochodzić m.in do przekazywania między nimi cząsteczek sygnałowych lub wspierających ich wzrost. Fimbrie umożliwiają również adhezję do powierzchni stałych. Tym samym uczestniczą w tworzeniu początkowych i dojrzałych form biofilmu. Fimbrie odgrywają więc istotną rolę w procesie infekcji. Mimo że znamy ich budowę molekularną, a także główne patogeniczne funkcje, to niestety nie rozumiemy procesów, które prowadzą do ich wydzielenia (tzw. sekrecji) i ekspozycji na powierzchni bakterii. Cząsteczki fimbrii są produkowane wewnątrz bakterii i nie mogą spontanicznie przechodzić przez błonę zewnętrzną. Musi istnieć specjalny system białkowy umożliwiający ich sekrecję, którego dokładna charakterystyka pomogłaby stworzyć związek hamujący ten proces, a przez to ograniczający patogenność P. gingivalis.
Tajemniczy mechanizm
Opisywane fimbrie są zbudowane z wielu elementów (podjednostek białkowych) zwanych fimbrylinami. Te w większości powstają z cząsteczek, które są lipoproteinami, czyli białkami, które są związane z cząsteczką lipidu (tłuszczu). Lipoproteiny są białkami powszechnie występującymi u bakterii Gram-ujemnych. Są produkowane w cytoplazmie. Ich cząsteczka posiada tzw. peptyd sygnałowy, czyli krótki fragment, który zawiera informację, gdzie daną cząsteczkę należy przenieść – do konkretnego miejsca w komórce lub poza nią. Dzięki specjalnym systemom transportującym cząsteczki przechodzą przez błonę wewnętrzną do peryplazmy. Tam peptyd sygnałowy jest usuwany przez odpowiedni enzym. Do nowo powstałego końca skróconej cząsteczki są przyłączane trzy łańcuchy lipidowe. Lipidy działają jak kotwica dla związanych z nimi cząsteczek białek. Niektóre lipoproteiny zakotwiczają się w błonach wewnątrz bakterii. Inne, w tym prekursory podjednostek fimbrii P. gingivalis, są przerzucane na drugą stronę błony zewnętrznej. Nowej lokalizacji zawdzięczają swoją nazwę – lipoproteiny powierzchniowe.
Mechanizmy, które leżą u podstawy ostatniego z możliwych etapów podróży białka, czyli sekrecji, są bardzo zróżnicowane i jak dotąd opisane dla stosunkowo niewielkiej liczby cząsteczek. Zwykle wymagają one utworzenia wyspecjalizowanego, mniej lub bardziej złożonego kanału białkowego (systemu sekrecji), przez które na zewnątrz są transportowane konkretne białka niczym przez tubę zakończoną otworem. Jednakże do tej pory nie udało się znaleźć systemu sekrecji fimbrii u bakterii P. gingivalis. Prawdopodobnie jest on bardzo ważny dla tego patogenu, ponieważ oprócz podjednostek fimbrii bakterie te produkują również wiele innych lipoprotein powierzchniowych, które biorą udział m.in. w poborze składników odżywczych i hemu. Są więc kluczowe dla ich funkcjonowania.
W naszym laboratorium znaleziono białka tworzące system, który wydziela lipoproteiny i eksponuje je na powierzchni komórki. System udało się odkryć dzięki obserwacji, że mutanty P. gingivalis pozbawione białek budujących ten system nie posiadają fimbrii. Według dotychczasowych ustaleń system składa się z białka, tworzącego kanał w błonie zewnętrznej oraz oddziałującego z nim białka zlokalizowanego w peryplazmie. To drugie przypomina budową tzw. białka opiekuńcze, czyli cząsteczki, które pomagają innym białkom zachować odpowiedni kształt. Analiza bioinformatyczna wykazała, że podobne białka są również obecne w innych blisko spokrewnionych bakteriach. Może to oznaczać, że badany przez nas mechanizm jest uniwersalny, a więc ważny dla wielu mikroorganizmów.
Próba rozwikłania zagadki
W pierwszej kolejności zbadamy strukturę przestrzenną białek, które budują system transportujący. Tak jak każda cząsteczka białka, tak i one są łańcuchami utworzonymi z ogniw – reszt aminokwasowych. To, w jaki sposób łańcuchy układają się w przestrzeni, tworząc odpowiedni kształt, pozwala na odgadnięcie funkcji białka. Podobnie jest w przypadku kształtu narzędzia. Dzięki niemu przedmiot nadaje się do odpowiedniego zadania.
Żeby określić strukturę białek, wykorzystamy dwie wiodące metody badań strukturalnych: kriomikroskopię elektronową (cryo-EM) oraz krystalografię rentgenowską. W metodzie cryo-EM oczyszczone białka są mrożone w bardzo niskiej temperaturze na specjalnych siatkach. Umożliwia to uchwycenie białek w ich naturalnym ułożeniu w przestrzeni (konformacji). Dzięki tej metodzie można przeanalizować zmiany konformacji cząsteczek. Jest to możliwe dzięki wykorzystaniu mikroskopu elektronowego, który rejestruje tysiące zdjęć cząsteczek białka w różnych orientacjach. Zestawiając wyniki analiz, będziemy mogli ustalić, jak cząsteczka wygląda w trójwymiarze. Krystalografia rentgenowska wymaga innego podejścia. Korzystając z tej metody, należy najpierw uzyskać kryształy białek, czyli mówiąc kolokwialnie – uwięzić cząsteczkę w formie kryształu. Często jest to proces trudny i czasochłonny. Uzyskane kryształy są następnie poddawane działaniu promieniowania rentgenowskiego, którego fale uginają się na krystalicznej strukturze. To uginanie (dyfrakcja) zależy od kąta padania promieniowania oraz układu chmury elektronów pochodzących z atomów budujących badane cząsteczki. Poszczególne obrazy dyfrakcyjne są rejestrowane. W oparciu o wyniki jest wyznaczana tzw. mapa gęstości elektronowej kryształu, wskazująca, gdzie znajdują się zagęszczenia elektronów. Na podstawie dalszej analizy wyznacza się położenie poszczególnych atomów tworzących wykrystalizowane białko, co umożliwia uzyskanie jego trójwymiarowej struktury.

A. Podczas analizy próbki
zapisuje się tysiące filmów
siatek, na których białka
są umieszczone. W tym
przypadku wybrano
opisywany w artykule
system sekrecji lipoprotein
uchwycony podczas
wydzielania fimbrii. Dla tej
konkretnej próbki można
otrzymać strukturę fimbrii,
z kolei analiza struktury
samego systemu sekrecji
wymaga optymalizacji
warunków.
B. W dalszych pracach
są potrzebne specjalne
oprogramowanie
i superszybkie komputery
dostępne w Polsce dzięki
platformie PLGrid.
Ta umożliwia wybór
rodzaju analizowanych
cząsteczek, w tym
przypadku fimbrii.
C. Na podstawie
dwuwymiarowego obrazu
oprogramowanie tworzy
trójwymiarowy obraz.
D. Jeśli dane są dobrej jakości,
to po kolejnych krokach
optymalizacji można
uzyskać model atomowy
cząsteczki, w którym widać
różne detale struktury. Przy
najwyższej rozdzielczości
można zobaczyć położenie
poszczególnych atomów,
przy niższych – ogólny
kształt cząsteczki.
Obie metody mają swoje ograniczenia. Pierwsza z nich umożliwia uchwycenie dynamiki białka, jednakże technika ta nie nadaje się do wyznaczania struktur małych białek. Ponadto uzyskiwana rozdzielczość jest zazwyczaj gorsza niż w krystalografii. Z kolei krystalografia rentgenowska pozwala na uzyskanie struktury o wiele wyraźniejszej (o lepszej rozdzielczości), niestety w tym przypadku tylko w takim przestrzennym ułożeniu, w jakim udało się uwięzić białko w krysztale (brak zatem informacji o dynamice). Trzeba jednak pamiętać, że białko unieruchomione w krysztale nie zawsze oddaje swój naturalny stan. Dlatego wykorzystanie obu metod umożliwia najbardziej kompleksową analizę struktury cząsteczek i dostarcza najwięcej informacji.
W dalszej części projektu planujemy również identyfikację innych białek zaangażowanych w transport lipoprotein na powierzchnię komórki. Przeanalizujemy białka, które przejściowo z nimi oddziałują. Ponadto chcemy określić, z jakich ogniw (reszt aminokwasowych) składa się wspomniany wcześniej peptyd sygnałowy. Kiedy poznamy jego sekwencję, będziemy mogli zidentyfikować także pozostałe lipoproteiny powierzchniowe u tych bakterii. Jest to szczególnie istotne, ponieważ z uwagi na ich lokalizację powierzchniową białka te są znakomitymi kandydatami do produkcji szczepionek. W dobie rosnącej antybiotykooporności może to stanowić atrakcyjną metodę zapobiegania infekcjom i ich skutkom.
Badania prowadzone w ramach finansowanego przez Narodowe Centrum Nauki projektu nr UMO-2023/51/D/ NZ1/02675, którego kierownikiem jest dr inż. Mariusz Madej.
Publikacja częściowo powstała w ramach przedsięwzięcia Ministra Edukacji i Nauki „Wsparcie prowadzenia badań naukowych i prac rozwojowych z wykorzystaniem infrastruktury badawczej Narodowego Centrum Promieniowania Synchrotronowego SOLARIS” na podstawie umowy nr 1/SOL/2021/2. Prezentowane w niej badania zostały wykonane w Centrum SOLARIS na kriomikroskopie elektronowym. Chcielibyśmy podziękować Michałowi Rawskiemu, Grzegorzowi Ważnemu i Marcinowi Jaciukowi za wsparcie.
Składamy serdeczne podziękowania polskiej infrastrukturze obliczeniowej wysokiej wydajności PLGrid (Centrum HPC: ACK Cyfronet AGH) za udostępnienie zaplecza komputerowego i wsparcia w ramach grantu obliczeniowego nr PLG/2024/017163.
Chcesz wiedzieć więcej?
Dominy S.S. et al., Porphyromonas gingivalis in Alzheimer’s disease brains: Evidence for disease causation and treatment with small- molecule inhibitors, „Science Advances” 2019, vol. 5(1), doi.org/10.1126/ sciadv.aau3333
Enersen M., Nakano K., Amano A., Porphyromonas gingivalis fimbriae, „Journal of Oral Microbiolog” 2013, vol. 5, doi.org/10.3402/jom. v5i0.20265
Shibata S. et al., Structure of polymerized type V pilin reveals assembly mechanism involving protease-mediated strand exchange, „Nature Microbiology” 2020, vol. 5(6), doi.org/10.1038/s41564-020- 0705-1

