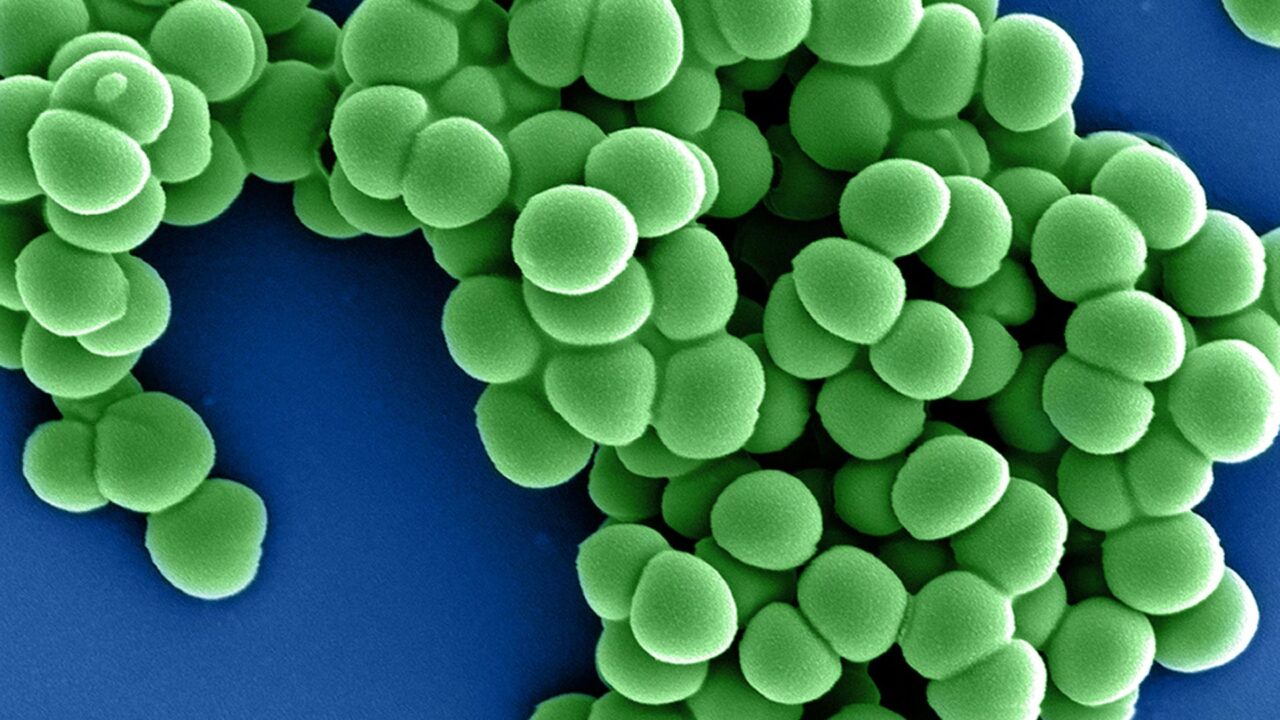
Kolorowany obraz z mikroskopu skaningowego przedstawiający bakterie Staphylococcus aureus oporne na metycylinę (MRSA). Zielone skupiska drobnoustrojów należą do jednych z najgroźniejszych patogenów szpitalnych, odpowiedzialnych za trudne w leczeniu zakażenia.
Fot. NIAID / Wikimedia Commons (CC BY 2.0)
Osiem dekad temu Aleksander Fleming, odkrywca penicyliny i jeden z ojców nowoczesnej antybiotykoterapii, odbierając Nagrodę Nobla ostrzegał przed konsekwencjami nieprzemyślanego stosowania antybiotyków. Przewidywał, że bakterie z czasem nauczą się je omijać. Dziś wiemy, że miał rację i że skala problemu znacznie przekroczyła jego najśmielsze obawy
W 2021 roku antybiotykooporność (AMR) bezpośrednio przyczyniła się do śmierci około 1,28 mln osób, a pośrednio – do ponad 5 mln kolejnych zgonów. Najnowszy raport WHO GLASS z 2025 r. potwierdza ten trend: w wielu regionach świata oporność na kluczowe leki osiągnęła już poziom krytyczny.
Naturalną reakcją wydaje się poszukiwanie nowych antybiotyków. Problem w tym, że od ponad czterech dekad nauka tkwi w tzw. „próżni odkryć” (discovery void). Ostatnie zupełnie nowe klasy antybiotyków opisano w latach 80., a większość współczesnych leków to jedynie modyfikacje znanych wcześniej związków. Co więcej, droga od odkrycia substancji do jej zastosowania klinicznego trwa nawet 15 lat.
W efekcie lekarze coraz częściej sięgają po rozwiązania awaryjne – terapie skojarzeniowe, antybiotyki „ostatniej szansy” czy leki o wysokiej toksyczności. To jednak strategia obronna, a nie trwałe rozwiązanie problemu.
Bakteriofagi – naturalni wrogowie bakterii
W naturze istnieje jednak mechanizm, który od milionów lat reguluje liczebność bakterii. Są nim bakteriofagi – wirusy wyspecjalizowane w infekowaniu komórek bakteryjnych.
Już w XIX w. Ernest Hankin zaobserwował w wodach Gangesu czynnik niszczący przecinkowce cholery. Dwie dekady później Félix d’Herelle zidentyfikował go jako wirusy i nazwał bakteriofagami. Dziś wiemy, że są one najliczniejszymi bytami biologicznymi na Ziemi. Towarzyszą nam na co dzień – znajdują się w wodzie, żywności, a także w naszym organizmie, wszędzie tam, gdzie obecne są bakterie: w jelitach, drogach oddechowych czy układzie moczowym.
Ich działanie jest precyzyjne. Bakteriofag rozpoznaje określony szczep bakterii, przyłącza się do jego powierzchni, a następnie wprowadza do wnętrza swój materiał genetyczny. Przejmuje aparat komórkowy gospodarza i wykorzystuje go do namnażania, często doprowadzając do zniszczenia komórki.
Ewolucyjny wyścig zbrojeń
Relacja bakterii i fagów to przykład nieustannego wyścigu ewolucyjnego. Bakterie wykształciły liczne mechanizmy obronne – od systemu CRISPR-Cas9 po strategie „samobójcze”, które mają ograniczyć rozprzestrzenianie się infekcji.
Fagi jednak nie pozostają w tyle. Jako organizmy zdolne do szybkiej ewolucji, odpowiadają na zmiany bakterii własnymi mutacjami. W przeciwieństwie do statycznych antybiotyków są dynamicznym narzędziem biologicznym, które może adaptować się do nowych warunków.
To właśnie ta zdolność sprawia, że oporność bakterii na fagi rozwija się inaczej niż w przypadku antybiotyków – i potencjalnie wolniej.
Od Tbilisi po Wrocław
Zastosowanie bakteriofagów w medycynie nie jest nowym pomysłem. Terapie fagowe rozwijano intensywnie w krajach byłego bloku wschodniego. Najbardziej znanym ośrodkiem jest Instytut Eliavy w Tbilisi. W Polsce badania i leczenie prowadzi m.in. Instytut Immunologii i Terapii Doświadczalnej im. Ludwika Hirszfelda PAN we Wrocławiu, gdzie fagoterapia stosowana jest w ramach procedur eksperymentalnych.
Największym wyzwaniem pozostają regulacje prawne. Fagoterapia ma charakter silnie spersonalizowany – skuteczność leczenia zależy od dopasowania wirusa do konkretnego szczepu bakterii u danego pacjenta. Tymczasem obowiązujące przepisy wymagają, aby lek miał stały i niezmienny skład.
Nie tylko medycyna
Potencjał bakteriofagów wykracza daleko poza leczenie ludzi. Już dziś stosuje się je w przemyśle spożywczym, np. do zwalczania bakterii Salmonella. Trwają również próby ich wykorzystania w rolnictwie, choć napotykają one trudności związane z wrażliwością fagów na warunki środowiskowe, takie jak promieniowanie UV czy zmiany temperatury.
Jednym z kierunków rozwoju są tzw. koktajle fagowe – mieszanki różnych wirusów, które zwiększają skuteczność działania i pozwalają zwalczać szersze spektrum bakterii.
Bakteriofagi nie są cudownym rozwiązaniem wszystkich problemów związanych z antybiotykoopornością. Wciąż wymagają intensywnych badań, zwłaszcza w kontekście ich wpływu na organizm człowieka i mikrobiotę.
Jednocześnie stanowią jedną z najbardziej obiecujących alternatyw w świecie, który zbliża się do granicy skuteczności klasycznych antybiotyków.
Nierozsądne stosowanie leków przeciwbakteryjnych doprowadziło nas na próg epoki postantybiotykowej. Pytanie, które dziś staje przed nauką i medycyną, brzmi nie tyle „czy”, ale „jak” wykorzystamy naturalnych wrogów bakterii, zanim będzie za późno.
Polecane:
-
Podcast
Mikrobiom jako klucz do zdrowia. Nowy odcinek podcastu PAN o bakteriach, które rządzą naszym ciałem Przejdź do publikacji: Mikrobiom jako klucz do zdrowia. Nowy odcinek podcastu PAN o bakteriach, które rządzą naszym ciałem
-
Podcast
Człowiek 2.0: Jak pomaga gorączka. Polka zmienia myślenie o szczepionkach Przejdź do publikacji: Człowiek 2.0: Jak pomaga gorączka. Polka zmienia myślenie o szczepionkach
-
Dlaczego warto zaprzyjaźnić się z swoim mikrobiomem i jak dbać o tę niezwykłą relację – już dziś w podcaście A o tym PAN słyszał? Przejdź do publikacji: Dlaczego warto zaprzyjaźnić się z swoim mikrobiomem i jak dbać o tę niezwykłą relację - już dziś w podcaście A o tym PAN słyszał?
Podobne artykuły
 Przejdź do publikacji: Badania bez szybkiego zwrotu. Czego Polska uczy się szybciej niż NASA
Przejdź do publikacji: Badania bez szybkiego zwrotu. Czego Polska uczy się szybciej niż NASA
Badania bez szybkiego zwrotu. Czego Polska uczy się szybciej niż NASA Przejdź do publikacji: Badania bez szybkiego zwrotu. Czego Polska uczy się szybciej niż NASA
 Przejdź do publikacji: Chemia biologiczna, chemia społeczna
Przejdź do publikacji: Chemia biologiczna, chemia społeczna
Chemia biologiczna, chemia społeczna Przejdź do publikacji: Chemia biologiczna, chemia społeczna
 Przejdź do publikacji: Co najbardziej śmiercionośne zwierzę mówi o historii naszego gatunku
Przejdź do publikacji: Co najbardziej śmiercionośne zwierzę mówi o historii naszego gatunku