Komórka raka piersi sfotografowana w skaningowym mikroskopie elektronowym, ukazująca trójwymiarową strukturę jej powierzchni. Źródło: National Cancer Institute (NIH, USA), domena publiczna.
Artykuł
Nowa broń przeciw rakowi. Naukowcy nauczyli się wyciszać gen RAS, nie niszcząc zdrowych komórek
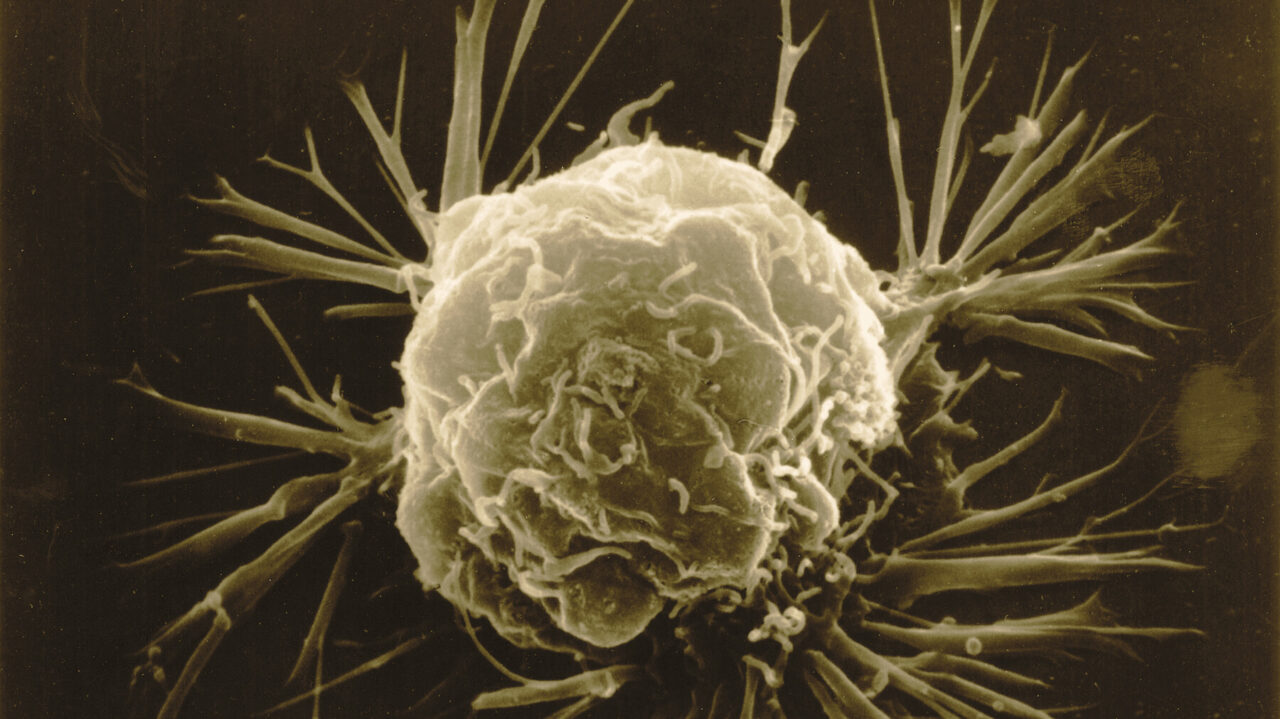
Badacze z Francis Crick Institute i Vividion Therapeutics opracowali nową klasę związków chemicznych, które blokują kluczowe interakcje białek napędzających rozwój raka. Lek właśnie trafił do pierwszej fazy badań klinicznych
Naukowcy z londyńskiego Francis Crick Institute oraz amerykańskiej firmy Vividion Therapeutics poinformowali o stworzeniu cząsteczek, które potrafią precyzyjnie zatrzymać sygnał wzrostu komórek nowotworowych – bez zakłócania pracy zdrowych tkanek. Wyniki badań opublikowano w Science, a potencjalny lek jest już testowany u ludzi.
RAS – gen, który nie zna umiaru
U podstaw wielu nowotworów leży mutacja genu RAS, odpowiedzialnego za uruchamianie ścieżek wzrostu komórek. W zdrowych tkankach RAS działa jak przełącznik – aktywuje podziały komórkowe tylko wtedy, gdy są potrzebne. Mutacja sprawia jednak, że białko RAS pozostaje stale „włączone”, nieustannie wysyłając sygnał rosnąć i dzielić się.
Szacuje się, że zmiany w genie RAS występują w około jednej piątej wszystkich przypadków raka – w tym raka płuca, jelita grubego i trzustki. Problem w tym, że całkowite zablokowanie aktywności RAS lub enzymów, które kontroluje, prowadzi do poważnych skutków ubocznych. Te same szlaki molekularne są bowiem niezbędne również dla zdrowych komórek.
Przykładem jest enzym PI3K, który oprócz interakcji z RAS uczestniczy też w działaniu insuliny i regulacji poziomu cukru we krwi. Jego zahamowanie może prowadzić do hiperglikemii.
Nowa strategia: przeciąć połączenie, nie wyłączyć układ
Zespół badaczy postanowił więc nie blokować całego białka, lecz przerwać jego kontakt z RAS. Dzięki połączeniu metod chemicznego „screeningu” z eksperymentami biologicznymi odkryto serię małych cząsteczek, które nieodwracalnie przyłączają się do powierzchni PI3K – dokładnie w miejscu, gdzie normalnie wiąże się RAS.
„Udało nam się zidentyfikować cząsteczki, które uniemożliwiają PI3K i RAS połączenie się, ale jednocześnie pozwalają PI3K działać w innych procesach, takich jak regulacja insuliny” – wyjaśnia prof. Julian Downward, kierownik grupy Oncogene Biology Laboratory w Francis Crick Institute. „To pozwala uniknąć efektów ubocznych, które dotychczas powstrzymywały rozwój skutecznych leków”.
W testach na myszach z guzami płuc zawierającymi mutację RAS nowy związek skutecznie zatrzymał wzrost nowotworów – i co ważne, nie powodował hiperglikemii.
Silniejszy efekt w terapii łączonej
Jeszcze lepsze rezultaty uzyskano, gdy eksperymentalny lek połączono z innymi inhibitorami szlaków RAS. Zastosowanie dwóch lub trzech preparatów jednocześnie doprowadziło do dłuższego i silniejszego zahamowania wzrostu guzów niż pojedyncze terapie.
Co więcej, nowy związek zadziałał również w nowotworach z mutacjami w genie HER2 – typowymi dla części raków piersi. W tym przypadku efekt nie zależał już od obecności RAS, co sugeruje, że opracowany inhibitor może znaleźć zastosowanie także w innych typach nowotworów.
„Odkrycie pokazuje, jak nowe podejścia w projektowaniu leków mogą otworzyć zupełnie inne drogi w walce z rakiem” – mówi dr Matt Patricelli, dyrektor naukowy Vividion Therapeutics. Zaprojektowaliśmy cząsteczki, które przerywają komunikację między RAS a PI3K, ale nie zakłócają funkcjonowania zdrowych komórek. To selektywne blokowanie sygnału wzrostu może przynieść realne korzyści pacjentom”.
Początek badań klinicznych
Nowy kandydat na lek trafił właśnie do pierwszej fazy badań klinicznych, które mają ocenić jego bezpieczeństwo i możliwe działania niepożądane u osób z mutacjami RAS lub HER2. Naukowcy będą też sprawdzać, czy połączenie nowego preparatu z innymi terapiami ukierunkowanymi na RAS daje lepsze efekty terapeutyczne.
Francis Crick Institute podkreśla w komunikacie, że projekt stanowi przykład skutecznej współpracy między nauką akademicką a przemysłem farmaceutycznym.
„To właśnie połączenie wiedzy chemicznej i biologicznej pozwoliło nam dojść do rozwiązania, które może realnie pomóc pacjentom z rakiem” – podsumowuje prof. Downward.
Źródła:
Francis Crick Institute, Science (2025), DOI: 10.1126/science.adv2684
Klebba, J. et al., Covalent inhibitors of the PI3Kα RAS binding domain impair tumor growth driven by RAS and HER2
Polecane:
-
Chemia, zdrowie, środowisko. Nowa jednostka badawcza PAN Przejdź do publikacji: Chemia, zdrowie, środowisko. Nowa jednostka badawcza PAN
-
Podcast
Chirurg na granicy życia i śmierci. Prof. Marek Krawczyk o tym, co czuje się przy stole operacyjnym Przejdź do publikacji: Chirurg na granicy życia i śmierci. Prof. Marek Krawczyk o tym, co czuje się przy stole operacyjnym
-
Artykuł
Flamingi zdradzają sekret długowieczności Przejdź do publikacji: Flamingi zdradzają sekret długowieczności
Podobne artykuły
 Przejdź do publikacji: Badanie krwi może przyspieszyć diagnozę ponad 50 rodzajów nowotworów
Przejdź do publikacji: Badanie krwi może przyspieszyć diagnozę ponad 50 rodzajów nowotworów
Artykuł
Badanie krwi może przyspieszyć diagnozę ponad 50 rodzajów nowotworów Przejdź do publikacji: Badanie krwi może przyspieszyć diagnozę ponad 50 rodzajów nowotworów
 Przejdź do publikacji: Co mówią geny o płci. Badania prof. Marka Świtońskiego
Przejdź do publikacji: Co mówią geny o płci. Badania prof. Marka Świtońskiego
Artykuł
Co mówią geny o płci. Badania prof. Marka Świtońskiego Przejdź do publikacji: Co mówią geny o płci. Badania prof. Marka Świtońskiego
 Przejdź do publikacji: Polscy naukowcy z grantami NCN: mikroglej i nowotwory w centrum uwagi
Przejdź do publikacji: Polscy naukowcy z grantami NCN: mikroglej i nowotwory w centrum uwagi
Artykuł