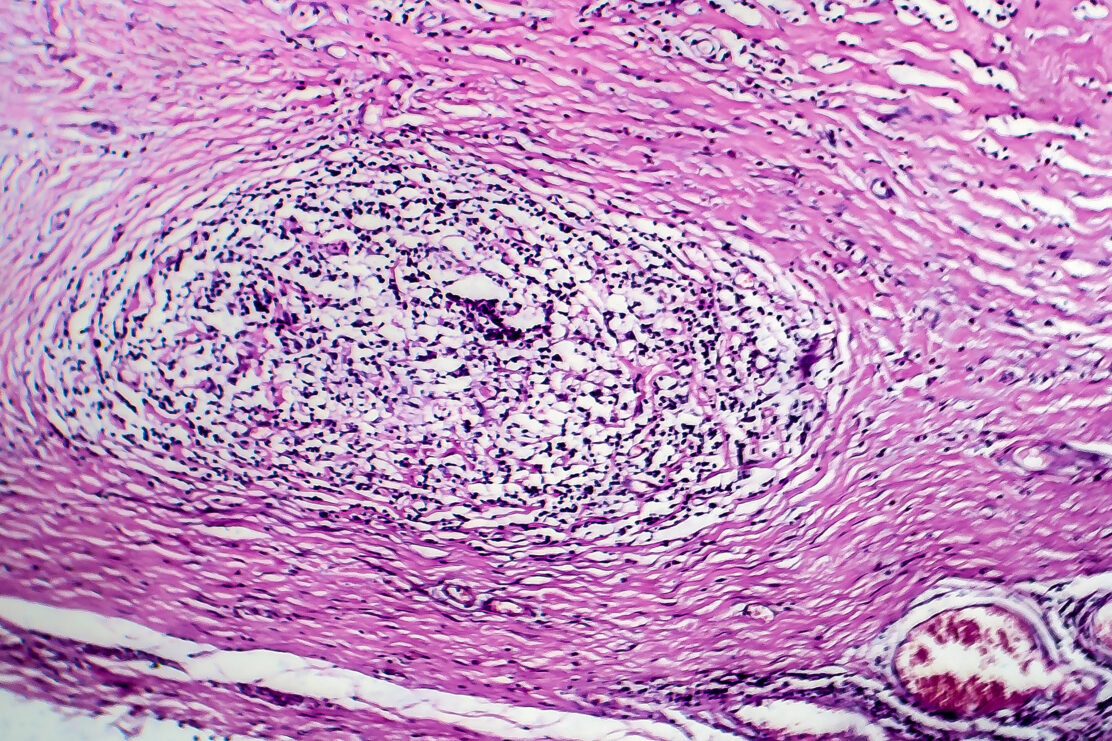
Nowe badania komórek odpornościowych przynoszą nadzieję na wynalezienie skutecznej terapii chłoniaka Hodgkina.
Chłoniak Hodgkina to nowotwór układu limfatycznego, który charakteryzuje się wysokim wskaźnikiem wyleczeń. Jednak nie zawsze tak było. Naukowcy w ciągu wielu lat opracowali terapie, które skuteczniej ratowały życie ludzi. Niestety, te są obciążone ciężkimi, potencjalnymi skutkami ubocznymi. Dzięki wykorzystaniu wyników międzynarodowych badań, w których uczestniczy polski zespół, może okazać się realne opracowanie efektywniejszych, lecz także bezpieczniejszych sposobów leczenia.
Jednym z podstawowych mechanizmów leżących u podstaw procesu tworzenia się nowotworów są zaburzenia w funkcjonowaniu białek nazywanych czynnikami transkrypcyjnymi.
Powiększone węzły chłonne wykazujące bolesność po spożyciu alkoholu, utrata masy ciała, poty nocne, długo utrzymująca się gorączka czy osłabienie – to mogą być niespecyficzne objawy klasycznego chłoniaka Hodgkina, znanego również w Polsce pod nazwą ziarnica złośliwa. Choroba ta charakteryzuje się niekontrolowanym rozrostem zmienionych nowotworowo komórek układu odpornościowego – limfocytów B. Dzieje się to w węzłach chłonnych, a także w śledzionie i innych organach w bardziej zaawansowanych stadiach choroby.
Sposoby leczenia
Postęp w leczeniu klasycznego chłoniaka Hodgkina może posłużyć jako przykład success story. Choroba stanowiąca znaczące wyzwanie kliniczne jeszcze w latach 60., gdzie pięcioletnie przeżycia oscylowały na poziomie 40 proc., charakteryzuje się obecnie bardzo dobrym rokowaniem. Sięga ono nawet 90 proc. w krajach rozwiniętych z dobrym dostępem do nowoczesnej terapii. Tak znaczny postęp w leczeniu został osiągnięty w ciągu kilku dekad i był możliwy dzięki wprowadzeniu wielotorowych działań. Należą do nich chemioterapia, radioterapia czy wysokodawkowa chemioterapia wspomagana przeszczepieniem krwiotwórczych komórek macierzystych. Należy podkreślić, że badania podstawowe, które były prowadzone w wielu laboratoriach na świecie, przyczyniły się do dobrego poznania zmian molekularnych w tej chorobie, umożliwiły w ostatnich latach wdrożenie do praktyki klinicznej immunoterapii. W efekcie ta nowoczesna terapia nie skupia się na komórkach nowotworowych per se, ale usprawnia działanie układu immunologicznego pacjenta w taki sposób, że rozpoznaje on i niszczy zmienione nowotworowo komórki.
Klasyczny chłoniak Hodgkina wyróżnia się dwoma szczytami zachorowań. Podobnie jak większość chorób nowotworowych diagnozuje się go częściej u ludzi starszych, głównie w okolicach 60. roku życia. Drugi szczyt zachorowań jest z kolei obserwowany w wieku nastoletnim lub u młodych dorosłych, w przedziale wiekowym 15–35 lat. Leczeniu poddaje się dużą liczbę młodych pacjentów, często przed okresem zakładania przez nich rodziny. Dlatego znacząca staje się kwestia toksyczności stosowanej terapii i jej skutków ubocznych w późniejszych dekadach życia. U takich pacjentów występuje podwyższone ryzyko wystąpienia drugich nowotworów pierwotnych po latach od pierwotnej diagnozy. Są one skutkiem uszkodzeń materiału genetycznego pacjenta po przebytym leczeniu. Dodatkowo istotny jest negatywny wpływ przebytego leczenia na płodność.
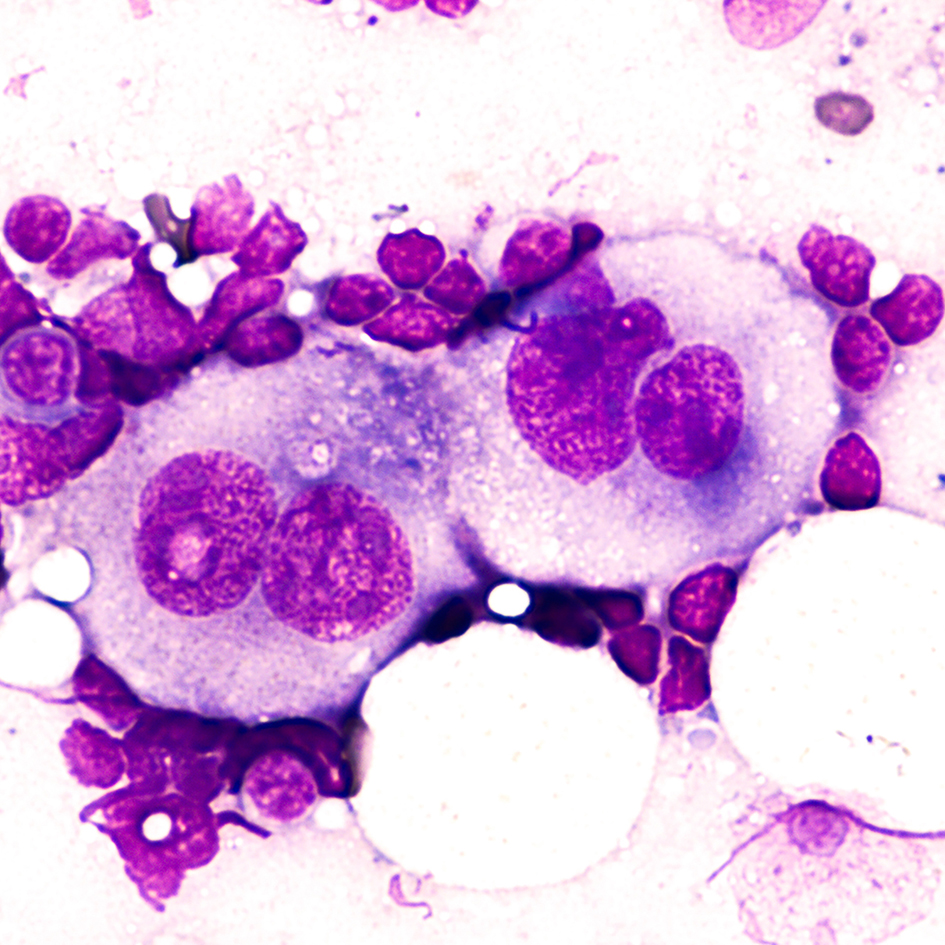
DAVID A LITMAN/SHUTTERSTOCK.COM
Połączone siły naukowe
Międzynarodowy zespół złożony z badaczy niemieckich z Instytutu Genetyki Człowieka Uniwersytetu w ULM i Max-Delbrück-Center for Molecular Medicine w Berlinie oraz polskich z Instytutu Genetyki Człowieka PAN w Poznaniu prowadzi owocną naukową współpracę, której celem jest zgłębianie zmian
skutkujących przemianą prawidłowego limfocytu B w komórki nowotworowe (nazywane komórkami Hodgkina i Reed-Sternberga – HRS). Są to zmiany zarówno genetyczne, jak i epigenetyczne, czyli modyfikujące aktywność genów w komórce, np. przez dołączanie do DNA niewielkich cząsteczek.
Jednym z podstawowych mechanizmów leżących u podstaw procesu tworzenia się nowotworów są zaburzenia w funkcjonowaniu białek nazywanych czynnikami transkrypcyjnymi. Białka te są swoistymi regulatorami aktywności genów, a ich zaburzenia pociągają za sobą lawinę zmian w komórce. W klasycznym chłoniaku Hodgkina obserwowano zarówno wzrost ich aktywności (np. czynnika transkrypcyjnego NFκB), jak i jej obniżenie (np. czynników transkrypcyjnych ETS1 i ELF1), co wykazała ta sama polsko-niemiecka grupa badaczy.
Jako cel obrano poszukiwanie mutacji aktywujących, a więc takich, które skutkują nadmierną aktywnością białka albo dodają nieprawidłowe funkcje zmienionemu białku. Spośród wielu potencjalnie interesujących genów, w których znaleziono mutacje, był także gen IRF4, który bierze udział w prawidłowym rozwoju plazmocytów. Plazmocytami nazywamy dojrzałe limfocyty B. Ich zadaniem jest produkcja przeciwciał służących do niszczenia patogenów. Badacze z Poznania na podstawie analiz teoretycznych nad strukturą i funkcją kodowanego białka postawili hipotezę, że znalezione zmiany na poziomie DNA mogą mieć istotne konsekwencje dla jego funkcjonowania. Takie przypuszczenie wynikało z tego, że w klasycznym chłoniaku Hodgkina białko IRF4 miało mutację (oznaczoną jako C99R) w bardzo ważnym miejscu cząsteczki, które odpowiadało za włączanie aktywności genów.
Wyniki te okazały się na tyle obiecujące, że prof. Stephan Mathas, lider grupy, rozpoczął szeroko zakrojone badania nad rolą uszkodzeń genu kodującego białko IRF4 w klasycznym chłoniaku Hodgkina. Do badań dołączyły kolejne grupy z Niemiec, a także z Wielkiej Brytanii, Kanady i Australii. Dzięki tak szerokiemu, wieloośrodkowemu działaniu możliwe było dogłębne poznanie znaczenia zidentyfikowanych mutacji genu IRF4.
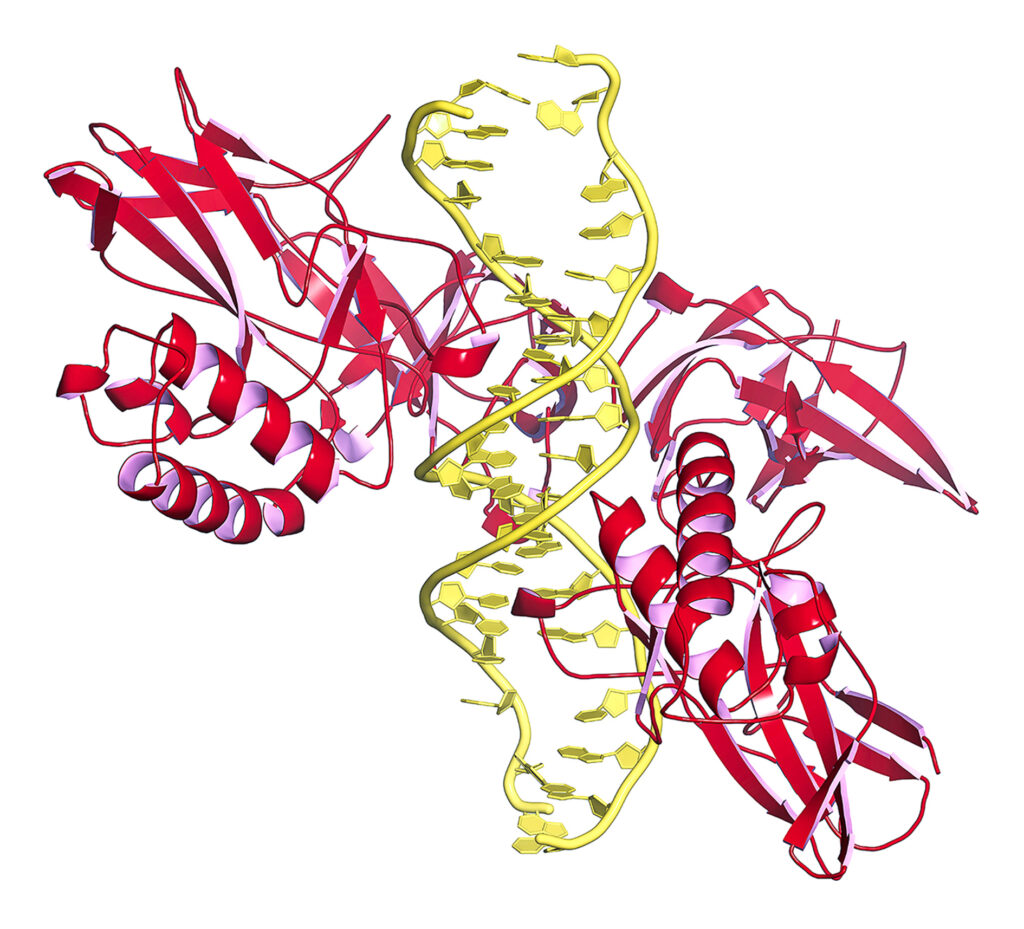
STUDIOMOLEKUUL/SHUTTERSTOCK.COM
Powstawanie mutacji
Ciekawy wydawał się fakt, że mimo wysokiej ekspresji IRF4 komórki HRS zatrzymują się w procesie dojrzewania, nie przekształcając się ostatecznie w plazmocyty. Ta pozorna sprzeczność została wyjaśniona przez prace powstałego konsorcjum. Wykazano bowiem, że mutacja C99R zaburza zdolność białka IRF4 do prawidłowego rozpoznawania regulowanych przez siebie genów. Z grupy prawie 300 prawidłowo rozpoznawanych genów pozostaje aktywowanych w tym procesie jedynie siedem. Równocześnie zmutowane białko aktywuje blisko 60 innych genów, które przeprogramowują komórkę i rozpoczynają proces jej przekształcania w komórkę nowotworową.
Należy podkreślić dwutorowy efekt opisanej mutacji. Z jednej strony jest ona typową mutacją, która wyłącza aktywność białka i zaburza prawidłowe rozpoznawanie genów przez IRF4. Z drugiej – dodaje także zmutowanemu białku nowe funkcje, czyli umożliwia rozpoznawanie innych genów niż w przypadku białka bez mutacji. Warte podkreślenia jest to, że wiele z niewłaściwie aktywowanych genów, w tym GATA3, CCL5 czy TNFRSF8 (CD30), pełni znane funkcje w klasycznym chłoniaku Hodgkina. Tym samym zidentyfikowana, pojedyncza mutacja C99R nie tylko skutkuje globalnym przeprogramowaniem komórki i przekształceniem jej w komórkę HRS. Tłumaczy ona zarazem, dlaczego komórki te charakteryzują się zablokowanym procesem dojrzewania w stronę plazmocytów.
Podsumowując, mutacja w genie IRF4 jest jednym z kluczowych elementów patogenezy molekularnej tego chłoniaka, ale wiadomo, że nie jedynym. Z przeprowadzonych badań wynika, że mutację C99R w komórkach HRS obserwuje się u 15‒20 proc. chorych. Dzięki przeprowadzonym badaniom patomechanizm warunkujący powstanie klasycznego chłoniaka Hodgkina stał się dużo bardziej zrozumiały. Oprócz tego poznanie miejsc wiązania zmutowanego białka IRF4 do DNA planuje się wykorzystać do opracowania nowych sposobów terapii klasycznego chłoniaka Hodgkina.
Chcesz wiedzieć więcej?
Schleussner N., Cauchy P., Franke V. et al., Transcriptional reprogramming by mutated IRF4 in lymphoma, „Nature Communications” 2023, vol. 14, doi.org/10.1038/s41467-023-41954-8
